Lukion taulukot/Molekyylien ja ionien muotoja
Ulkoasu
Molekyylien ja ionien muotoja
[muokkaa | muokkaa wikitekstiä]| Molekyylityyppi | Muoto[1] | Elektronimuodostelma[1] ml. vapaat parit vaaleankeltaisella |
Geometria[1] pl. vapaat parit |
Esimerkkejä |
|---|---|---|---|---|
| AX2E0 | Lineaarinen | BeCl2,[2] CO2[3] | ||
| AX2E1 | Taipunut | 
|

|
NO2-,[2] SO2,[1] O3,[2] CCl2 |
| AX2E2 | Taipunut | 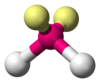
|

|
H2O,[1] OF2[4] |
| AX2E3 | Lineaarinen | 
|
XeF2,[1] I3-,[4] XeCl2 | |
| AX3E0 | Tasokolmio | 
|

|
BF3,[1] CO32-,[4] NO3-,[2] SO3[3] |
| AX3E1 | Trigonaalinen pyramidi | 
|

|
NH3,[1] PCl3[4] |
| AX3E2 | T-mallinen | 
|

|
ClF3,[1] BrF3[4] |
| AX4E0 | Tetraedrimäinen | 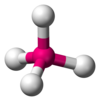
|

|
CH4,[1] PO43-, SO42-,[3] ClO4-,[2] XeO4[4] |
| AX4E1 | Disfenoidi | 
|
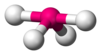
|
SF4[1][4] |
| AX4E2 | Tasoneliö | 
|

|
XeF4[1] |
| AX5E0 | Trigonaalinen bipyramidi | 
|

|
PCl5[1] |
| AX5E1 | Neliöpohjainen pyramidi | 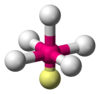
|

|
ClF5,[4] BrF5,[1] XeOF4[3] |
| AX5E2 | Tasomainen viisikulmio | 
|

|
XeF5-[4] |
| AX6E0 | Oktaedri | 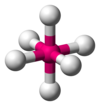
|

|
SF6[1] |
| AX6E1 | Pentagonaalinen pyramidi | 
|

|
XeOF5-,[5] IOF52-[5] |
| AX7E0 | Pentagonaalinen bipyramidi[3] | 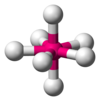
|

|
IF7[3] |
| AX8E0 | Neliömäinen antiprisma[3] | 
|

|
IF8- |
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 Petrucci, R. H. & Harwood, W. S. & Herring, F. G.: General Chemistry: Principles and Modern Applications. 8. painos. Prentice-Hall, 2002. ISBN 978-0-13-014329-7.
- ↑ 2,0 2,1 2,2 2,3 2,4 Jolly, W. L.: Modern Inorganic Chemistry. McGraw-Hill, 1984. ISBN 978-0-07-032760-3. Worldcat.
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 3,6 Miessler, G. L. & Tarr, D. A.: Inorganic Chemistry. 2. painos. Prentice-Hall, 1999. ISBN 978-0-13-841891-5.
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 4,7 4,8 Housecroft, C. E. & Sharpe, A. G.: Inorganic Chemistry. 2. painos. Pearson, 2005. ISBN 978-0-130-39913-7.
- ↑ 5,0 5,1 Baran, E.: Mean amplitudes of vibration of the pentagonal pyramidal XeOF5- and IOF52- anions. J. Fluorine Chem., 2000, nro 101. doi:10.1016/S0022-1139(99)00194-3.
